Abstrakt
Parametry krevního obrazu,
retikulocytů a diferenciálního rozpočtu leukocytů stanovené na automatickém
analyzátoru krevních buněk Sysmex XN-1000 metodou průtokové fluorescenční
cytometrie-FCM s polovodičovým laserem.
Seznam souvisejících dokumentů
Laboratorní
příručka
Příručka kvality
Provozní řád
Skartační řád
S-OKBH-004 Směrnice pro IKK-OKBH
S-OKBH-005 Směrnice EHK
PI-OKBH-31
Provedení kontrol hematologie
LP C-11 Informace
k transportu vzorků
SOPT –
Hematologický analyzátor Sysmex XN-1000
SOPV – Hodnocení
nátěru PK
PI-OKBH-86 Manuál Sysmex XN-1000
Kódy, názvy, definice a terminologie
Krevní
obraz a diferenciální rozpočet leukocytů, retikulocyty
Reagenční souprava: Roztoky a činidla v kapitole Reagencie
Název a
klíč v lokálním číselníků LIS: Krevní obraz 7 parametrů (BKO)
Krevní obraz a pětipopulační diferenciál (BKOD5)
Číslo metody v lokálním číselníku LIS: Krevní obraz 7 parametrů-722
Krevní
obraz a pětipopulační diferenciál-723
Seznam
zdravotních výkonů VZP:96163 Kompletní krevní obraz se 7 parametry (včetně
destiček)
96167 Stanovení
kompletního hemogramu a 5-ti populačního rozpočtu
Leukocytů
96857 Stanovení počtu retikulocytů na
automatickém analyzátoru
CBC = cell
blood count (picture) – krevní obraz (KO)
Forma
vydávání výsledků
|
WBC |
= white
blood cell count – leukocyty |
x.x [109/l] |
|
RBC |
= red
blood cell count – erytrocyty |
x.xx [1012/l] |
|
HGB |
=
hemoglobin |
x [g/l] |
|
HCT |
=
hematokrit (měřeno integrací napěťových pulzů |
x,xxx |
|
MCV |
= mean corpuscular
volume-střední objem erytrocytů, vypočtená hodnota dle vzorce: MCV=Hct/RBC |
xx.x
[fl] |
|
MCH |
= mean
corpuscular hemoglobin – barvivo v erytrocytu vypočtená hodnota dle vzorce: MCH
= Hgb / RBC |
xx.x
[pg] |
|
MCHC = množství hemoglobinu
v erytrocytární mase vypočtená hodnota:
MCHC=HGB/(HCT.1000)
xxx g/l |
||
|
RDW = red cell volume distribution width – šíře distribuce
erytrocytů
x.x [%] |
||
|
PLT = platelet count - krevní destičky x
[109/l] |
||
|
PCT = plateletcrite – destičkový hematokrit 0,xxx |
||
|
MPV = mean platelet volume – střední objem
trombocytů xx.x
[fl] |
||
|
|
||
|
PDW = platelet distribution width – šíře distribuce krevních
destiček xx.x
[%] |
||
|
|
||
|
NRBC = normoblasty
x.xx [109/l] v % |
||
|
|
||
|
RET = retikulocyty
x.xxx [1012/l] |
||
|
|
||
|
Ret-He = hemoglobin v retikulocytu
xx.x pg |
||
|
|
||
|
IPF = nezralé frakce trombocytů
xx.x % |
||
|
|
||
Princip
Impedanční princip
s hydrodynamickou fokusací
Měření probíhá v komoře, kam je nasát vzorek naředěný vodivým
diluentem. Přesně stanovené množství ředěného vzorku je pak pomocí vakua
z této komůrky nasáváno malým otvorem, jehož průměr je srovnatelný
s velikostí buňky. Po obvodu měřící kyvety protéká vyšší rychlostí vodící
kapalina (sheath reagent) a proudem nosné kapaliny jsou buňky unášeny a řazeny
za sebou. Otvorem (apertura) prochází stejnosměrný proud, který neproniká do
cytoplazmy. Při průchodu buňky je z plochy apertury vytlačena část
diluentu a změní se elektrický proud procházející aperturou. Tyto změny jsou
snímány jako impulsy, jejichž amplituda je přímo úměrná velikosti buňky.
Analyzátor tedy současně s počtem impulsů – s počtem procházejících
buněk – změří i jejich objem. Počet impulzů v přesném malém objemu
přepočte na objemovou jednotku, velikost impulsu zprůměruje a vydá ji jako
střední objem buňky. Softwarem lze stanovit meze velikosti typické pro určité
buňky, a tak lze současně při průchodu jednou aperturou měřit více druhů buněk
(erytrocyty a trombocyty).
Erytrocyty a trombocyty se stanoví ze stejného ředění vzorku
a jsou odlišeny velikostí buňky. Za trombocyt je považována buňka velikosti 1-4
µm, větší jsou začleněny mezi erytrocyty. Leukocyty jsou stanoveny
z menšího ředění a pro vyloučení rušivých vlivů erytrocytů a trombocytů je
do naředěného vzorku přidáváno lyzační činidlo, které lyzuje všechny buňky
(včetně leukocytů-dochází k částečnému nebo úplnému rozrušení cytoplazmy a
WBC se hodnotí v pozici částečného narušení membrány nebo se hodnotí jen
jádro). Počet impulzů a jejich velikost je roztříděna a graficky zobrazena ve
formě histogramu. Je to křivka, kde na ose x je amplituda impulzu – objem buňky
a na ose y počet stejně velkých impulsů – počet buněk. Ideálně má tvar Gaussovy
křivky.
Impedanční princip je využíván v analyzátorech největší
měrou. Jeho nevýhody vyplývají z principu a patří sem zejména interference
mezi různými typy buněk. Modernější automaty jsou schopny mnoho z těchto
interferencí odhalit, nebo alespoň textovou zprávou (flagg) na možnost
interference upozornit.
Stanovení hemoglobinu
Je stanovován
spektrofotometricky.
Měření se provádí z ředění
vzorku určeného pro počítání leukocytů. Po ukončení počítání leukocytů je
z lyzační komůrky převedeno přesně změřené množství vzorku do
hemoglobinového fotometru. Zde je vzorek opakovaně změřen při vlnové délce 540
nm. Dle míry absorpce světla je možné určit množství hemoglobinu a přepočtem i
jeho hladinu v původním vzorku plné krve. Stanovení je prováděno
několikrát, nejnižší a nejvyšší hladina je z průměru vynechána. Po
ukončení měření je komůrka vypláchnuta detergentem a ten je opět několikrát
proměřován – určí tzv. blank, se kterým je pak porovnávána absorbance světla
vzorkem.
SLS metoda měření
koncentrace hemoglobinu.
Látka
sodium lauril sulfát (SLS) obsažena v lyzačním činidle způsobí následné
chemické reakce – hemolýzu erytrocytů, konfirmační změny v molekule
globinu, oxidaci železa a vznik komplexu SLS – hemoglobin.
V
materiálu k měření hemoglobinu jsou přítomna i leukocytární jádra. Analyzátor
automaticky koriguje výpočtem hladinu hemoglobinu dle počtu leukocytů.
Leukocytosa v oblasti hraniční pro linearitu přístroje může hladinu hemoglobinu
ovlivnit. Vzorek je potřeba pak změřit naředěný.
Interference-chylosita
vzorku, leukocytosa.
Chylosní vzorek lze změřit v ředění, a
pokud ani toto nestačí, lze vzorek promýt. Po centrifugaci 5 minut při 1500 rpm
odsajeme vrstvu plazmy a přesně změříme její objem. Do vzorku přidáme stejný
objem diluentu. Někdy je nutné promýt vzorek opakovaně. Získaná hladina
hemoglobinu má větší chybu a je nutné na toto upozornit v poznámce vydávané
současně s výsledkem. Se změnou hodnoty hemoglobinu ve výsledku musíme i
přepočíst parametry vypočtené z hladiny hemoglobinu.
Optická metoda měření počtu leukocytů.
Kanál
pro leukocyty a bazofily: kyselé složky reagencie způsobí lýzu erytrocytů,
trombocytů a všech leukocytů (zůstanou tzv. holá jádra) kromě bazofilů. Po
expozici laserovým paprskem analyzátor snímá dva signály – rozptyl přímého
paprsku, jehož intenzita informuje o velikosti buňky a rozptyl bočního paprsku,
jehož intenzita informuje o vnitřní struktuře buňky a odseparuje tak populaci
bazofilů od ostatních leukocytů. Celkový počet leukocytů je dán součtem
bazofilů a ostatních leukocytů.
Stanovení
retikulocytů
optickou metodou spočívá v intravitálním obarvení (metylenová modř) a poté v
analýze vzorku laserem. Erytrocyty jsou, pokud nejsou lyzovány, zachyceny v
čidle 10°a retikulocyty ještě lomí a polarizují světlo-registrace 90°. Tato
dvojí registrace je pro retikulocyty s obarvenou RNA v plazmě typická a umožní
určit procento retikulocytů ve změřeném počtu erytrocytů. Stanovení absolutního
počtu je pouze přepočtem na počet erytrocytů.
Fluorescenční
průtoková cytometrie-optická metoda. Přístroj
využívá kombinace průtokové cytometrie a rozptylu laserového paprsku.
Princip: Velikost úhlu rozptylu přímého laserového
paprsku je přímo úměrná velikosti buňky (detektor Forward Scatter), intenzita
bočního rozptylu laserového paprsku je přímo úměrná hustotě vnitřní struktury
buňky (detektor Side Scatter) a intenzita fluorescenčního záření vycházející
z buňky je přímo úměrná aktivitě a nepřímo úměrná stupni vyzrálosti buňky
(detektor Side Fluorescence Light.
Fluoreccenční průtoková cytometrie využívá dvou měřících
systémů ke stanovení buněk, každý z nich využívá jiné lyzační činidlo
s různou účinností a odlišné způsoby detekce buněčných populací:
a) měřící systém (channel) ke stanovení neutrofilů,
eozinofilů, monocytů a lymfocytů
b) měřící systém (channel) ke stanovení bazofilů.
ada) lyzační činidlo způsobí destrukci RBC a PLT a
perforuje membránu WBC, kterou pronikne barvivo,které
se váže na
DNA, RNA v jádře a cytoplazmě (intenzita fluorescence odpovídá množství
nukl.kyselin),
intenzita
bočního rozptylu informuje o členitosti jádra a obsahu granulí, organické
kyseliny v lyzačním
činidle se
specificky váží k eozinofilním granulím a tím jsou odlišeny od neutrofilů,
velikost signálu je
úměrná
objemu buněk, počet detekovaných buněk (jader)odpovídá počtu WBC
adb) kyselé složky lyzačního činidla způsobí lýzu RBC,
PLT, WBC (zůstanou holá jádra) kromě basofilů
(jsou
větší a komplexnější než holá jádra ostatních WBC)
Celkový počet WBC je dán součtem basofilů a ostatních
leukocytů.
Místo provádění postupu
OKBH, úsek
hematologie, Nemocnice AGEL Ostrava-Vítkovice a.s.
Zalužanského 1192/15,70384 Ostrava-Vítkovice
Bezpečnostní aspekty
Je nutné dodržovat obecné zásady
bezpečnosti práce podle ČSN 01 8003, směrnice VN BOZP č.8.02, ale i zásady
práce s biologickým materiálem, který může být zdrojem přenosu některých
infekcí. Zejména je třeba zachovávat pravidla osobní hygieny, používat osobní
ochranné pracovní prostředky (oděv, obuv a podobně), při práci nejíst, nepít
a nekouřit. Po práci a před jídlem omýt pokožku především rukou teplou
vodou a mýdlem a ošetřit vhodným reparačním krémem. Při zasažení očí
vymývat velkým množstvím vlažné vody nejméně 15 minut. Při zasažení oděvu a
kůže odložit veškeré kontaminované oblečení. Okamžitě kůži omýt velkým
množstvím, pokud možno vlažné vody, popř. mýdlem nebo jiným vhodným mycím
prostředkem. Po umytí ošetřit vhodným reparačním krémem. S-OKBH-003 Směrnice o
práci s biologickým materiálem
Fáze před vyšetřením
Výsledky
krevního obrazu poskytují informaci nejen o počtu, ale také o velikosti a
některých dalších charakteristikách krevních buněk. Krev se skládá z krevních
buněk rozptýlených v tekutině nazývané plazma. Tyto buňky (zralé červené a bílé
krvinky a krevní destičky) jsou produkovány kostní dření a uvolňovány dle
potřeby organismu do krevního oběhu. Doplňujícími vyšetřeními krevního obrazu
mohou být nátěr periferní krve a diferenciální rozpočet leukocytů.
Odběr primárního vzorku a transport
Odběr
Odběr
se provádí standardním způsobem ze žilní krve, do plastové zkumavky s K3EDTA,
K2EDTA,
pro obvyklé
vyšetřování je vhodný odběr ráno, nevyžadují se striktní dietní opatření.
Pro stanovení trombocytů
k vyloučení pseudotrombocytopenie se provede odběr krve do speciální
zkumavky
(Monovette TromboExact f.Sarstedt) nebo zkumavky s citrátem sodným (1:9).
Transport
Transport materiálu na oddělení OKBH VTN je popsán
v laboratorní příručce LP
C-11 Informace k transportu vzorků. Transport materiálu musí být
šetrný, rychlý, při teplotě +15 až+
Skladování
Zkumavka se vzorkem se po provedení analýzy skladuje při
+15 až +
Interference
Extrémní lipémie, vysoký bilirubin,
chylomikrony, hemolýza.
Stabilita
+15 až+25°C: 5 hodin
Omezení
Laboratoř
může odmítnout přijetí materiálu a neprovést požadované vyšetření
z obecných důvodů uvedených v Laboratorní příručce v kapitole
Kritéria pro přijetí nebo odmítnutí primárních vzorků.
Nedostatečné
promíchání, nesprávné skladování a transport může vést k nesprávným
výsledkům.
V případě
nesprávného odběru a vzniku sraženiny ve vzorku není stanovení provedeno.
Interference
a limity:
1.
Některé natrvalo srpkovité buňky, které se objevují v případě srpkovité anémie,
se nemusí v systému zcela seskupit, čehož výsledkem je zvýšené RDW a tím pádem
podhodnocení MCV. Srpkovité buňky mohou způsobit chybné výsledky u dalších
parametrů RBC.
2.
Velmi vysoké počty WBC (>100 x 10³ buněk/μl) zvyšují počet RBC,
HGB a HCT
3.Vzorky
s chladovými aglutininy mohou mylně snížit počet RBC, HCT, falešně zvýšené
MCHC
4.
Vzorky s extrémní lipémií, chylomikrony nebo extrémně vysokým bilirubinem mohou
způsobit interferenci a zvýšit výsledky HGB, falešně zvýšené MCHC.
5.
Vzorky pacienta s jadernými RBC-rezistentní vůči lýze, NRBL (zejména neonatální
vzorky) mohou mylně zvýšit počet WBC
6.
Vzorky pacientů, kteří dostávají úplnou parenterální výživu (TPN) včetně
podávání vysokých dávek lipidů, mohou způsobit mylně zvýšené počty krevních
destiček. Tyto vzorky mohou zahrnovat kapénky lipidů, které se objevují v
oblasti počítání krevních destiček, a tím zvýšit počet krevních destiček.
7.Snížený
počet PLT-pseudotrombocytopenie-způsobuje antikoagulační roztok, shluky PLT a
velké PLT
8.Zvýšený
počet PLT způsobují fragmenty RBC, WBC a mikro RBC.
9.Snížení
WBC-způsobuje agregace WBC, zvýšení WBC způsobují shluky PLT
10.Mikroerytrocyty
a fragmenty RBC snižují počet RBC a HCT
11.Abnormální
proteiny zvyšují HGB.
12.Urémie,
silný diabetes a sférocytoza zvyšují HCT.
13.
Agregace RBC, velké PLT, shluky PLT, fragmenty WBC, Howell-Jollyho těl. mohou
zvyšovat RET
14. Pseudohyperkalémie: Při
hodnotě WBC> 50 109/l nebo PLT> 1000 109/l dochází
k falešnému zvýšení draslíku. Při hodnotě K> 5,5 mmol/l doporučujeme
odběr plazmy (heparin).
Manipulace se vzorky
Pro uzavřený
i otevřený systém je použita jedna aspirační jehla. Vzorek je před měřením
nutné promíchat převracením-ne třepáním. Před uložením do podavače je nutné
každý vzorek prohlédnout na přítomnost sraženin, vzorky na vyšetření krevního
obrazu měříme nejdříve po 15-20 min. po odběru, při vyšetření diferenciálního
rozpočtu leukocytů po 30 min. od odběru, aby došlo k vyrovnání
koncentračních gradientů po styku s antikoagulantem.
Přístroje a
pomůcky
Sysmex XN-1000
- automat s měřením krevního obrazu s 5-ti populačním diferenciálem a
retikulocyty,
s možností
měření vzorků z podavače uzavřeným modem, nebo s otevřeným způsobem
měření.
Reagencie
Výrobce
– Sysmex s.r.o, Elgartova 683/4,614 00 Brno
Zásadně je nutné užívat originální
reagencie doporučené pro typ přístroje, jsou určené k přímému použití.
Kat.č.
Cellpack
DCL CT661628
Sulfolyser
SLS 904-1141-4
Cellclean
CL-50 934-0172-9
Cellpack
DFL BT965910
Fluorocell
PLT CD994563
Fluorocell
RET BN337547
Fluorocell
WDF CV377552
Fluorocell
WNR CP066715
LyserCell
WDF AL337564
LyserCell
WNR BL121531
Skladování: Reagencie jsou skladovány při +15 až +
Stabilita: Reagencie jsou stabilní do doby exspirace, která
je uvedena na každém balení. Stabilita v přístroji
při +15až+30º C 90dnů.
Manipulace
s reagencií: Reagencie jsou připraveny k přímému použití, výměna
reagencií se provede dle
pracovní instrukce PI-OKBH
Způsob
likvidace: Likviduje se jako biologický materiál.
Spotřební
materiál
Ochranné rukavice
Čistící prostředek-Savo
Další spotřební materiál dle aktuální potřeby dodaný firmou
Příprava k činnosti
Provede se denní údržba dle pracovní instrukce PI-OKBH- Manuál Sysmex XN-
.
Pracovní postup
Viz.SOPT
– Hematologický analyzátor Sysmex XN-1000
Viz.PI-OKBH-86
Manuál Sysmex XN-1000
Vzorky je
možné zpracovat v tzv. otevřeném nebo uzavřeném systému. Při otevřeném
zpracování se materiál promíchá, vkládá se každý vzorek jednotlivě, a to buď
uzavřený, nebo otevřený obsluhou. Při práci v uzavřeném systému ukládáme
zkumavky se vzorky do racku a ty vložíme do podávacího prostoru analyzátoru.
Vzorky jsou dopravovány, míchány, aspirovány a analyzovány.
Stručný popis postupu
1. zapneme přístroj (jednotka IPU) probíhá automaticky inicializace přístroje a kontrola jednotlivých
částí (mikroprocesor, mechanické části, teplota, tlak a pozadí).
2.
provedeme denní kontrolu kvality
3.
zkumavky vložíme do racku a umístíme do podavače
4.
výsledky jsou průběžně odesílány do LIS a validovány obsluhou
Kalibrace a návaznost
Přístroje
jsou výrobcem kalibrovány, a pokud jsou výsledky průběžné kontroly kvality v
referenčních mezích, není nutné kalibraci opakovat. Případné doladění je možné
změnou jednotlivých kalibračních faktorů.
Charakteristika spolehlivosti
Charakteristika
spolehlivosti viz. manuál Sysmex XN-1000.
Variační koeficienty
přesnosti
|
Parametr |
|
|
WBC |
do 3,0% |
|
RBC |
do 1,5% |
|
HGB |
do 1,0% |
|
HCT |
do 1,5% |
|
MCV |
do 1,0% |
|
PLT |
do 4,0% |
Aktuální
charakteristiky spolehlivosti:
Aktuální charakteristika
spolehlivosti je uvedena v platném verifikačním protokolu pro parametry
krevního obrazu pro analyzátor Sysmex XN-1000.
Dokumentace, výpočty, zpracování dat a
vydávání výsledků
Primární
výsledky vyšetření z analyzátorů se automaticky zálohují na síťové
uložiště NAOV.
Výsledky vyšetření zanesené v LIS laboratoře se
archivují v elektronické podobě.
Likvidace se řídí skartačním řádem.
Lékařům na odděleních a ambulancích Nemocnice Agel
Ostrava Vítkovice a.s. jsou výsledky vyšetření k dispozici elektronicky
v NIS a v případě potřeby v tištěné podobě na OKBH.
Spolupracujícím lékařům jsou výsledky zasílány
průběžně elektronicky a následující den doručovány v tištěné podobě
se svozem biologického materiálu.
Výsledková zpráva obsahuje:
·
identifikaci laboratoře, která výsledek
vydala
·
odkaz na akreditaci laboratoře
·
datum a čas vydání nálezu
·
jednoznačnou identifikaci pacienta
·
zdravotní pojišťovnu pacienta
·
identifikaci požadujícího subjektu (lokalizaci pacienta,
je-li to vhodné)
·
identifikaci požadujícího lékaře (resp. oddělení)
·
diagnózu pacienta
·
druh biologického materiálu (sérum, plazma, moč, krev u vyšetření
krevního obrazu)
·
jasně srozumitelnou identifikaci vyšetření
·
datum a čas přijetí vzorku laboratoří
·
datum a čas odběru vzorku
·
výsledek vyšetření s odpovídajícími jednotkami (nejčastěji SI
jednotky)
·
označení akreditované metody
·
referenční intervaly vyšetření
·
interpretaci výsledků, je-li to nutné
·
jiné poznámky (např. kvalita nebo dostatečnost primárního vzorku,
pokud tato může nežádoucím způsobem ovlivnit výsledek požadovaného vyšetření)
·
identifikaci osob, které výsledkovou zprávu kontrolovaly a
schválily
·
zkratky identifikující žádanku
·
př. 20.BR-0777
·
20: den v měsíci, BR: biochemie rutina, 0777: číslo vzorku
·
př. 20.HH-0777
·
20: den v měsíci, HH: hematologie, 0777: číslo vzorku
Referenční a varovná rozmezí
Referenční hodnoty u zdravé populace s ohledem na věk dle
doporučení ČHS.
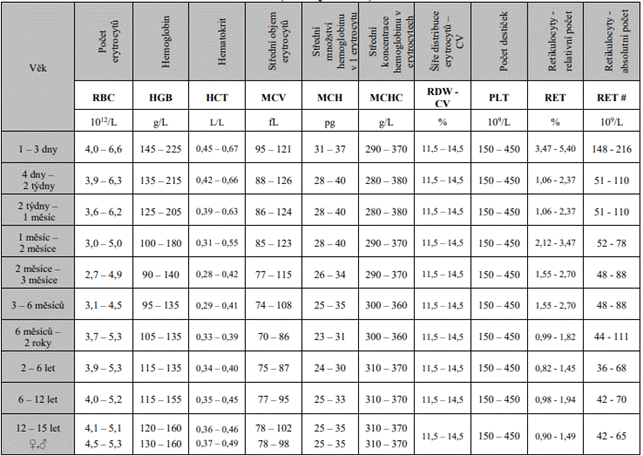
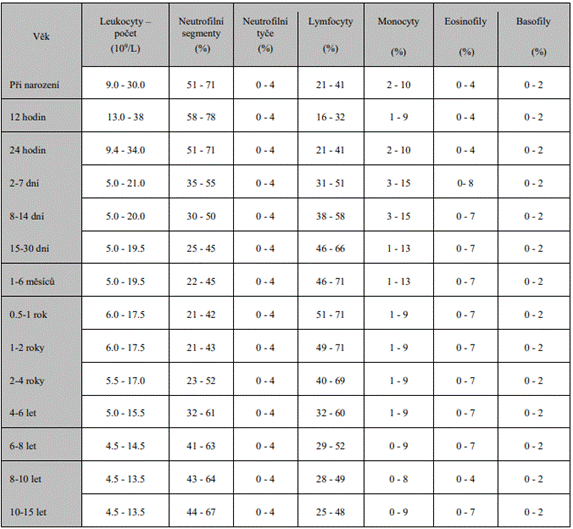
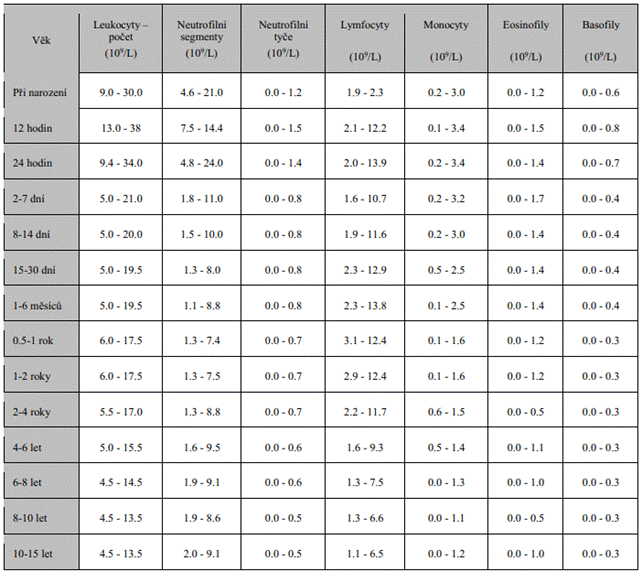
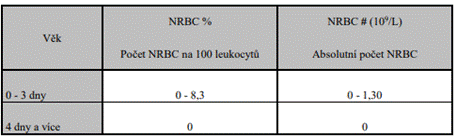
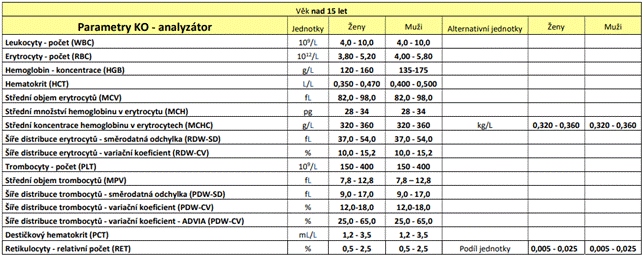
![]()
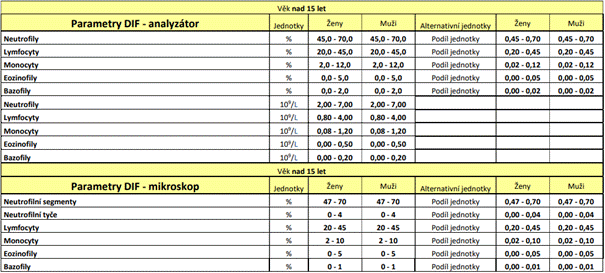
Interpretace výsledků, konzultační
činnosti a hlášení
Krevní
obraz je běžné vyšetření, které se provádí k určení zdravotního stavu. Pokud se
počty krvinek nachází ve fyziologickém rozmezí, další krevní obraz se provádí
až při změně zdravotního stavu.
Vyšetření krevního obrazu se provádí k odhalení příčiny v případě, že má
pacient symptomy jako jsou únava, slabost, infekce, podlitiny,
krvácení. V případě zvýšení bílých krvinek je lékař schopen potvrdit přítomnost
infekce a provést další testy k odhalení její lokalizace a původce. U sníženého
počtu červených krvinek – anémie – jsou dále vyšetřovány změny velikosti a
tvaru červených krvinek, které mohou napomoci odhalit příčinu. Tou může být
snížení produkce, zvýšení ztrát, nebo zvýšení destrukce červených krvinek. V
případě vyššího počtu krevních destiček lze odhalit riziko trombotických stavů.
V případě nižšího počtu pak zvýšené riziko krvácení. Změny v počtu krevních
destiček (PLT) provází i hematologická onemocnění, např. leukémii. Mnoho stavů může vést ke zvýšení nebo snížení
počtu krevních buněk. Některé nemoci, jako jsou onkologická onemocnění (léčená
chemoterapií) mohou ovlivnit produkci krevních buněk kostní dření a zvýšit
produkci jednoho typu buněk na úkor jiného, nebo celkově snížit produkci
krevních buněk. Některé léky mohou snížit počet bílých krvinek. Nedostatek
některých vitamínů a minerálů může způsobit anémii.
Krevní obraz se provádí též k monitorování průběhu nemoci a ke kontrole léčby.
Diferenciální
rozpočet bílých krvinek – rozlišení typů bílých krvinek. Každý má svoji funkci
v ochraně těla proti infekci: neutrofily, bazofily, eosinofily, lymfocyty a monocyty.
Leukocytóza – zvýšený
počet leukocytů. Výskyt u infekční a zánětlivých on., leukemie,
lymfoproliferativní on., myeloproliferativní on., otrav, popálenin,
těhotenství, krvácení.
Leukopenie – snížený
počet leukocytů. Výskyt u dřeňových útlumů, některé infekce, léčba
imunosupresivy, leukemie (HCL, APL ..)
Neutrofilie – zvýšený
počet neutrofilů. Výskyt u bakteriálních infekcí, zánětlivých on.,
myeloproliferativních on., těhotenství
Neutropenie – snížený
počet neutrofilů. Výskyt u při poruchách imunity, u dřeňových útlumů,některých
infektů, leukemie
Agranulocytóza –
snížení až vymizení granulocytů. Výskyt u polékové agranulocytózy, dřeňové
útlumy, protinádorová léčba, leukemie
Lymfocytóza – zvýšený
počet lymfocytů. Výskyt u virových infekcí, leukemie, lymfoproliferativní on.
Lymfopenie – snížený
počet lymfocytů. Výskyt u některých infekcí, po ozáření, intoxikaci.
Eozinofilie – zvýšený
počet eozinofilů. Výskyt při alergiích, parazitárních on.,
myeloproliferativních on.
Bazofilie – zvýšený
počet bazofilů. Výskyt u alergií, CML.
Monocytóza – zvýšený
počet monocytů. Výskyt u MDS, chronických inf., virových inf., leukemie
Trombocytóza –
sekundárně zvýšené hodnoty trombocytů. Výskyt u zánětu, stresu, léčba
kortikoidy, traumata, krvácení, nádorová on., autoimunitní on.
Trombocytemie –
primárně zvýšené hodnoty trombocytů. Výskyt u myeloproliferativních on.
Tromobytopenie –
snížený počet trombocytů. Výskyt u imunosupresivní léčby, leukemie,
lymfoproliferativní on., myeloproliferativní on., krvácení, protilátky proti
trombocytům, protinádorová léčba, alkoholizmus, plastická anémie, TTP, DIC,
HUS, HIT, HELLP syndrom, septické stavy, hypersplenismus
Erytrocyty
·
Snížené-anémie, dřeňový útlum, leukemie, krvácení,
lymfoproliferativní on., myeloproliferativní on
·
Zvýšené–polyglobulie, polycytémie
Hemoglobin
·
snížený-anémie
·
zvýšený –
polycytémie,polyglobulie
Hematokrit
·
snížený/zvýšený u
podobných stavů,u kterých se vyskytují změny v erytrocytech
MCV
·
slouží
k rozlišení mikrocytární,normocytární,makrocytární anémie
MCH
·
slouží
k rozlišení anémie hypochromní,normochromní a hyperchromní
MCHC
·
snížení u hypochromní
a makrocytární anémie
·
zvýšení u hereditární
sférocytózy
RDW
·
zvýšení u anizocytózy
erytrocytů,slouží k odlišení talasemie od sideropenické anémie
Řízení kvality
Interní
kontrola kvality je zajištěna měřením firemních kontrolních vzorků na 3
hladinách dle pracovní instrukce PI-OKBH-31 Vnitřní
kontrola kvality-KO vycházející z doporučení ČHS ČLS JEP-Vnitřní kontrola kvality měření krevních obrazů
na hematologických analyzátorech.
Příprava: Kontrolní materiál je uchováván při +2až+8ºC v lednici. Po vytemperování na laboratorní
teplotu a
promíchání je připraven
k použití.
Stabilita: Při +2až+8 ºC je stabilní do doby exspirace, po otevření je stabilní 7
dnů.
Externí kontrola
kvality v rámci České republiky je organizována společností SEKK, směrnice S-OKBH-005 Směrnice EHK
Dokumentace: Výsledky denních
kontrol se archivují v SW analyzátoru, elektronicky se přenášejí
do LIS a programu Unity Real Time. V LIS jsou rovněž validovány
vedoucími úseku
Poznámky, zdroje variability
Počet eozinofilů a monocytů bývá lehce vyšší než při
mikroskopickém hodnocení.
Analyzátor není schopen rozlišit jednotlivé formy
neutrofilů
Analyzátor
dále v případě patologií vydává morfologické hlášky (flags) informující o
snížení nebo zvýšení počtu buněk, výskytu různých anomálií nebo shluků PLT.
Meze parametrů, při kterých se zhotovuje nátěr
|
|
Parametr |
hodnota |
|
Bílá řada |
Leukocytóza Leukopenie |
≥ 30 x 109/l ≤ 2
x 109/l(neléč.) |
|
|
Lymfocytóza |
≥ 60 % nebo 10 x 109/l |
|
|
Monocytóza |
≥ 20 % |
|
|
Nezralé granulocyty (IG) |
přítomny |
|
|
Abnormální lymfocyty |
přítomny |
|
|
Blasty |
přítomny |
|
|
Pancytopenie |
WBC <4, HGB <120
PLT <100 |
|
Červená řada |
Normoblasty (NRBC) |
≥ 10 % |
|
PLT |
|
<100x109/lpři prvozáchytu <50 x 109/l hodnotit současně i schistocyty(≥10hlásit lékaři) shluky PLT |
Kódy,
názvy jednotlivých parametrů krevního obrazu v lokálním číselníku:
Kód Klíč Název
705 BLE Leukocyty
706 BERYPR Erytrocyty
708 BHB Hemoglobin
709 BHTC Hematokrit
710 BMCV Střední
objem erytrocytů
712 BMCH Střední
množství hemoglobinu v erytrocytu
713 BMCHC Střední
koncentrace hemoglobinu v erytrocytech
714 BRDW-CV Šíře
distribuce erytrocytů – variační koeficient
715 BTRPR Trombocyty
716 BMPV Střední
objem trombocytů
717 BNE Neutrolily
718 BEO Eozinofily
719 BBA Bazofily
720 BMO Monocyty
721 BLY Lymfocyty
971 NRBC Normoblasty
790 BRET Retikulocyty
981 QFI102 Ret-He-Hemoglobin
v retikulocytu
982 QFI103 IPF-Frakce nezralých
trombocytů
Jiné související informace
Nevyplněno
Literatura
·
SLP
·
Pecka, M.: Přehled
laboratorní hematologie II, Galén, 1996.
·
Pecka, M.: Přehled
laboratorní hematologie IV, Galén, 2000.
·
Doporučení ČHS ČLS JEP
„Referenční meze krevního obrazu, retikulocytů, normoblastů a diferenciálního
počtu leukocytů u dětí, 2023
·
Doporučení ČHS ČLS JEP
„Referenční meze krevního obrazu, etikulocytů, normoblastů a diferenciálního
počtu leukocytů u dospělých, 2021
·
Doporučení ČHS ČLS
JEP-Vnitřní kontrola kvality měření krevních obrazů na hematologických
analyzátorech, 2022
·
XN series (XN-1000)
-Pokyny pro použití
·
Hematologický systém
Sysmex XN-1000 – Příručka operátora
·
Doporučení
ČHS ČLS JEP Preanalytika v hematologické laboratoři, 2021
·
Ricos C, Alvarez V, Cava F,
Garcia-Lario JV, Hernandez A, Jimenez CV, Minchinela J, Perich C, Simon M.
"Current databases on biologic variation: pros, cons and progress."
Scand J Clin Lab Invest 1999;59:491-500.2014
Appendixy
Nevyplněno
Autorské poznámky
nevyplněno
Recenze, schválení
Autor: Mgr. Eva Miková